核酸医薬品のLC-MS/MSによる生体試料中濃度測定

低吸着仕様のHPLCと高感度MS/MSを組み合わせたシステムのポテンシャルを最大限に引き出し、核酸医薬品の迅速な分析法の開発と、信頼性の高い測定を実現します。
背景
核酸医薬品は、従来の低分子医薬品やバイオ医薬品では治療が困難であった疾患に対する次世代の治療アプローチとして期待されています。
様々な夾雑物を含む生体試料中の薬物濃度測定には、高感度で選択性の高いLC‑MS/MSが有用であり、有効成分である核酸だけでなく、その代謝体などの関連成分も同時に測定することが可能です。一方で、核酸特有の構造・物性に起因する吸着の課題により、分析が困難となる場合があります。
当社は、AMED(国立研究開発法人日本医療研究開発機構)事業「4種の新規モダリティ医薬品を対象とする薬物動態評価のための生体試料中濃度等分析法の開発と標準化に関する研究(令和4~6年度)」に参画し、核酸医薬品のLC-MS/MS測定における課題解決に取り組んでいます。
特長
吸着の影響で高感度での測定が難しい核酸医薬品に対しても、前処理やLC条件(イオンペア試薬の選定など)を最適化することで、キャリーオーバーを低減し、高い真度および精度での定量を実現します。
- 各種規制(GLP・信頼性基準)に準拠し、ICH-M10(International Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use-M10): 生体試料中薬物濃度分析法バリデーションおよび実試料分析に関するガイドラインに適合した生体試料中の薬物濃度測定を実施します。
- 新薬の探索段階での細胞毒性評価、抗薬物抗体(Antibody-Drug Conjugate: ADC)測定、サイトカイン測定、被験物質としての特性試験および品質試験など、核酸医薬品の研究開発で必要となる各種サービスをワンストップでご提供します。
事例
ICH-M10では、生体試料中の薬物濃度分析法のバリデーションと実際の試料分析に関する要求事項が定められており、ICH-M10に適合した分析法が求められます。以下、ICH-M10要求事項への対応事例を示します。
モデル化合物
Fomivirsen
- アンチセンス核酸医薬品
- Phosphorothioate(PS)修飾
- MW 6682.4
- 5'-GCGTTTGCTCTTCTTCTTGCG-3’(21塩基)
要求事項と適合性
定量範囲 2.00~1000 ng/mL
- 直線性 適合
- 真度 適合
- 精度 適合
- 選択性 適合
- キャリーオーバー 適合
測定機器
HPLC:Nexera™ XS inert(Shimadzu Corp.)
MS:Triple Quad™ 7500(AB Sciex Pte. Ltd.)
クロマトグラム
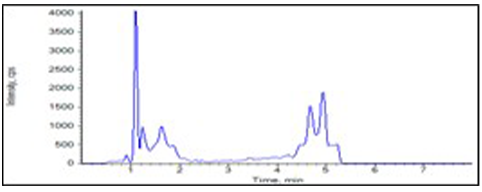
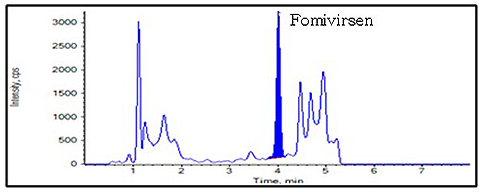
真度(Accuracy)および精度(Precision)
| Nominal Conc. (ng/mL) |
2 | 5 | 300 | 800 |
|---|---|---|---|---|
| Determined Conc.(ng/mL) | 2.1 | 4.62 | 324 | 832 |
| 1.83 | 4.77 | 315 | 845 | |
| 1.94 | 4.25 | 304 | 803 | |
| Mean | 1.96 | 4.55 | 314 | 827 |
| S.D. | 0.14 | 0.27 | 10 | 22 |
| Precision (%) | 6.9 | 5.9 | 3.2 | 2.6 |
| Accuracy (%) | 97.8 | 90.9 | 104.8 | 103.3 |
核酸医薬品関連測定
その他、核酸医薬品開発に必要な関連分析に対応いたします。
| ADA(Anti-drug Antibody)測定 | ELISA(Enzyme-Linked Immuno-Sorbent Assay)法、ECL(Electrochemiluminescence)法、SPR(Surface Plasmon Resonance)法 |
| サイトカイン測定 | ELISA法(EllaTM(自動化機器)含む)、ECL法 |
| 特性試験 | 性状、定量、確認試験、純度試験(類縁物質)、生物活性 |
| 毒性スクリーニング | 細胞毒性、ご要望により光毒性、in vitro小核試験も実施可 |
参照
- GLP(厚生省令第21号)「医薬品の安全性に関する非臨床試験の実施の基準に関する省令」
- 信頼性基準実施体制(医薬品、医療機器等の品質、有効性および安全性の確保等に関する法律施行規則第43条)
- GCP(厚生省令第28号)「医薬品の臨床試験の実施の基準に関する省令」
- 独立行政法人医薬品医療機器総合機構、 “ICH-M10 生体試料中薬物濃度分析法バリデーション及び実試料分析”、 <000272440.pdf>、(accessed 2025.11.28)
技術事例
お問い合わせ・ご相談
