医薬品原薬のPDE(ADE)/OEL設定

医薬品の製造設備における交叉汚染防止および作業者安全のリスク管理のために
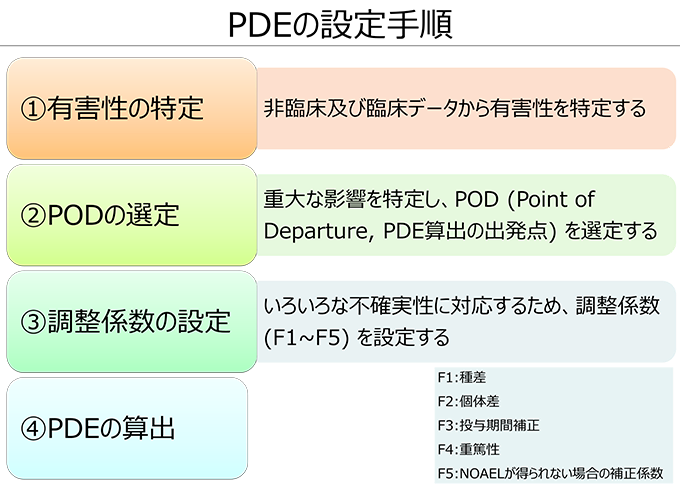
医薬品の製造設備の共用において、交叉汚染リスク管理は避けられない課題です。PDE*は、人が一生涯毎日摂取したとしても健康に影響がないと考えられる毒性学的根拠に基づく用量上限値であり、医薬品製造における交叉汚染防止限度値の算出に利用されます。
PIC/S GMPガイドライン(2018年施行)等において、毒性学的根拠に基づく交叉汚染防止限度値の設定が義務化され、PDEの設定の重要性が高まっています。
当社では、PDE設定を行うために必要な毒性学の知識と豊富な経験を有する専門家により、PDE設定方針のご相談から報告書作成まで対応可能です。
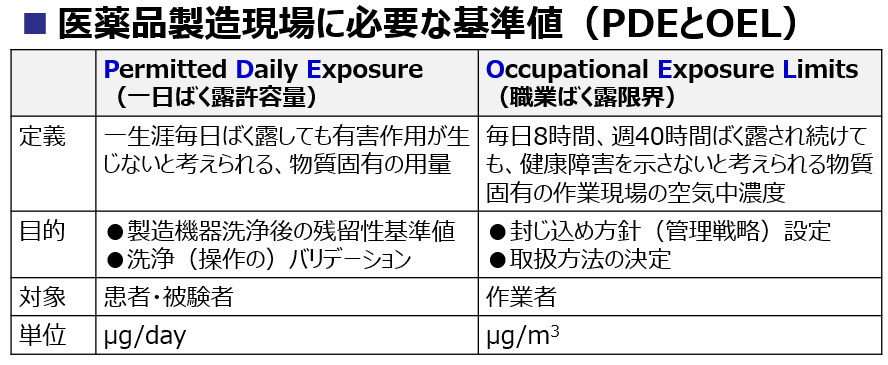
PDEとともに医薬品製造現場に必要な基準値であるOEL**の算出も対応可能です。
*Permitted daily exposure: 一日ばく露許容量/ADE(Acceptable Daily Exposure)と同意
** Occupational Exposure Limit:職業ばく露限界

当社は、国際製薬技術協会(ISPE)日本本部のPDE設定検討会***のメンバーとして、最新動向を情報収集しています。
2018年PIC/S発出のHBEL設定ガイドラインの記載内容を補完する解説書 「ゼロから学ぶHBEL!共用施設における医薬品の交叉汚染防止のためのPDE設定」 (2021年発行 PDE設定検討会/編著 じほう)にて、当社の毒性学専門家は共同執筆をしました。
***PDE設定に関する国内製薬業界でのハーモナイズと専門家の育成を目的に2017年にスタート
適用ガイドライン
- EMA Guideline (2014). Guideline on setting health based exposure limits for use in risk identifi cation in the manufacture of diff erent medicinal products in shared facilities (EMA/CHMP/CVMP/SWP/169430/2012).
- EU GMP (2014). EudraLex – Volume 4 Good manufacturing practice (GMP) guidelines, Chapter 3 and Chapter 5.
- PIC/S GMP (2018). Guideline on setting health based exposure limits for use in risk identifi cation in the manufacture of diff erent medicinal products in shared facilities (PIC/S, PI 046-1 Annex, 1 July 2018).
- PIC/S GMP (2020). Questions and answers on implementation of risk-based prevention of cross-contamination in production and guideline on setting health-based exposure limits for use in risk identifi cation in the manufacture of diff erent medicinal products in shared facilities (PIC/S, PI 053-1, 1 June 2020).
- ASTM international (2020). ASTM E3219-20. Standard guide for derivation of health-based exposure limits (HBELs).
- GMP省令 (2021). 厚生労働省令第九十号 (令和3年4月28日) 医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令, 第8条の2, 及び第9条第1項第5号、第9条第2項.
ご相談やご依頼につきまして、ご要望に合わせて丁寧に対応いたします。
PDE/OEL設定に関するご質問やご相談がございましたら、お気軽にお問い合わせください。
技術事例
お問い合わせ・ご相談
