医薬品原材料の中国ドラッグマスターファイル登録支援サービス

中国国家薬品監督管理局/医薬品評価センター(NMPA/CDE)へのDMF(Drug Master File/ドラッグマスターファイル)登録に関する
あらゆる手続きを、経験豊富な専門家がワンストップでサポートします。
製薬メーカーが中国に医薬品を申請する際の添加剤や包装材などのDMF登録に係る様々なお悩みのご相談も承ります。
医療機器材料のマスターファイル登録も可能です。
サービス内容
1.DMFの登録支援 ~作成から登録まで一貫してサポートします~
お客様のお悩みやご要望に合わせた最適なサービスをご提案します。

2.中国公定書準拠試験の実施
中国要件に適合した試験のご提案
中国薬局方とのGAP分析を行い、追加で実施すべき試験項目をご提案します。

中国要件に適合した試験の実施
中国試験施設で中国薬局方準拠試験や包装材の中国YBB規定準拠試験を実施し、試験結果を速やかにDMFに反映します。
必要に応じて試験報告書(中国語)の日本語への翻訳も承ります。

3.審査対応 ~DMF登録後の審査対応も安心してお任せください~
LOA(Letter of Authorization/参照許可証)の作成
NMPA/CDEが審査の際にDMFを参照するために必要な許可証(LOA)の作成を支援します。
DMFを登録しただけでは審査は行われません。製薬メーカーがLOAを添付し、医薬品を申請してはじめてDMFの審査が始まります。

審査対応
NMPA/CDEからの照会事項に対し、回答方針のご提案、回答書作成、DMFの改訂をサポートします。

4.DMFの維持・管理 ~毎年必要となる手続きもお任せください~
DMFの年次更新・変更手続き(Annual Report、Amendment)
最新情報であることを当局に知らせる年次更新対応や、登録情報に変更が生じた場合に必要となる変更手続きも対応します。
年次更新は毎年1~3月の間に提出する必要があります。

問い合わせ対応
ご不明な点がございましたら、何でもご相談ください。NMPA/CDEへの問い合わせも代行します。

実績
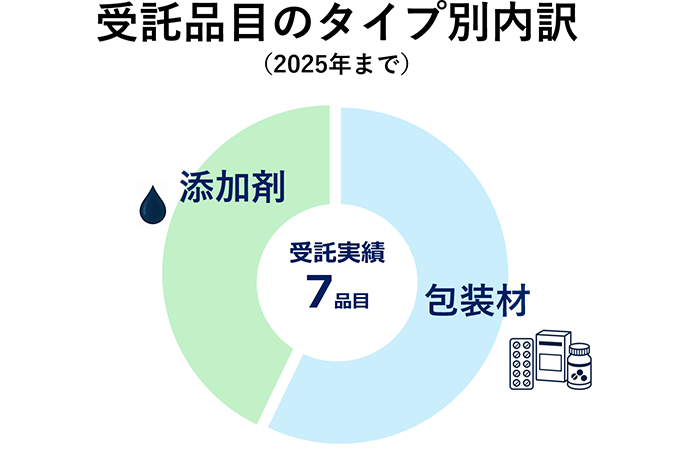
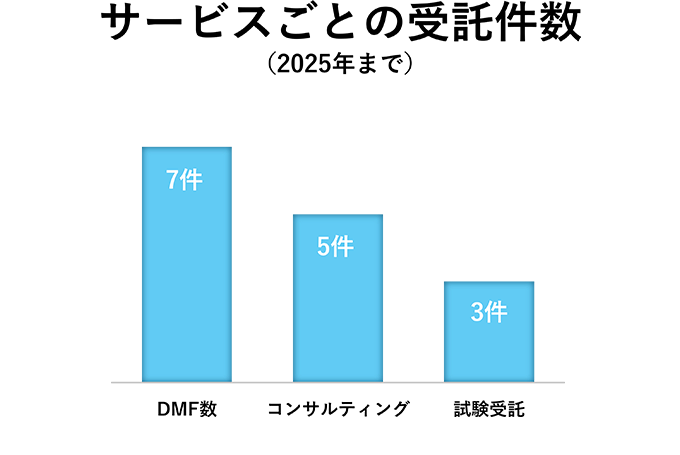
当社の強み

現地パートナーとの強力な連携
中国現地の信頼できる複数のパートナーと協力し、迅速かつ的確に対応します。

専門家によるコンサルティング
医薬品製造・品質管理・薬事など多様なバックグラウンドを持つ専門家が、最適な解決策をご提案します。

豊富な実績
中国に新規参入されるお客様を含め、様々な業種のお客様からDMF登録のご依頼をいただいています。

厳格な品質管理
徹底したQCチェックにより信頼性の高いサービスをご提供します。
よくあるご質問
Q.DMF登録は初めてですが、大丈夫でしょうか?
A. はい、中国薬事規制の基礎から必要な記載情報まで、分かりやすくご説明しながらサポートします。
Q.DMF登録に必要な準備期間はどれくらいですか?
A.正式にご依頼いただいてから概ね1年ぐらいで登録可能ですが、データの充足度によって異なるため、ヒアリングを元に最短、最適なプランをご提示します。米国、欧州あるいは日本にDMFを登録済の場合は準備期間を短縮できる可能性がありますが、中国での試験が必要なケースが多いので、通常は1年以上かかってしまうことも多いです。
Q.日本で承認取得した製剤を中国に申請したい。原薬や添加剤、包装材のDMF登録をサポートしてもらえますか?
A. はい、そういったサポートにも経験があります。まずはお問い合わせフォームよりご相談ください。最適な方法をご提案します。
Q.当社の製品はどの申請カテゴリーになるでしょうか?
A. 同じ投与経路で上市医薬品に既に使用されている場合は、薬局方への収載状況(中国薬局方や日本薬局方(JP)/米国薬局方(USP)/欧州薬局方(EP)/英国薬局方(BP))により、以下のいずれかのカテゴリーになりますが、投与経路が異なる場合や新規製品の場合は、リスクに応じて別のカテゴリーになります。最終的には詳細情報をご提供いただき、現地パートナーにも確認の上、適切な申請カテゴリーをご提案します。製品によってはDMFに登録できない場合もございますので、まずはお問い合わせフォームよりご相談ください。
包装材
4.1 中国での登録証明書のない医薬品包装材
4.2 中国での登録証明書のある医薬品包装材
添加剤
2.1 中国薬局方/USP/EP/BP/JPのいずれにも収載されていない添加剤
2.2 USP/EP/BP/JPのいずれかに収載されているが、中国国内の上市医薬品に使用されていない添加剤
2.3 USP/EP/BP/JPのいずれかに収載されているが、中国薬局方に収載されていない添加剤
2.4 中国薬局方に既に収載されている添加剤
Q. 証明書類に関して、公証が必要と聞いていますが、どのように対応したらよいでしょうか?
A. 公文書か私文書かによって対応が変わります。ご相談いただけましたら、公証が必要な書類ごとに適切な対応をご提案します。
Q. 日本で原薬等登録原簿(MF)に登録している資料を使って中国にDMF登録したいが、追加で何が必要でしょうか?
A. まずはMFの内容をレビューさせていただき、不足する情報があればご提案します。
Q. 試験は日本薬局方(日局)で行っていますが、中国薬局方の試験も必要でしょうか?
A. 日局と中国薬典のGAP分析を行い、追加で実施が必要な試験項目があればご提案します。現地パートナーを通じて、中国当局による認定を受けた試験施設で試験を行うことも可能です。
Q.当局への電子申請は対応可能でしょうか?
A.はい、対応可能です。2024年3月よりCD-ROMを用いた当局申請が行われております。現地委託先を通じた対応実績が御座います。
Q.具体的な相談の前に料金を知りたいです。
A.DMF登録される製品の種類や資料のボリューム、ご希望されるサービス内容によるため、ヒアリングをさせていただいた上でお見積りをご提示しています。まずはお問い合わせフォームよりご連絡ください。ご予算に応じたサービスをご提案します。
関連サービス
中国向け原薬のDMF登録については以下を参照ください。
技術情報
技術事例
お問い合わせ・ご相談
