欧州薬局方(EP)収載品のマスターファイル(CEP)登録支援サービス

欧州評議会欧州医薬品医療品質部門(EDQM)へのCEP(Certificate of Suitability to the monographs of the European Pharmacopoeia)登録に関する
あらゆる手続きを、経験豊富な専門家がワンストップでサポートします。
欧州薬局方(EP)に収載されているものであれば、原薬でも添加剤でも登録できます。
サービス内容
1.CEPの登録支援 ~CEPの作成から審査対応、登録まで一貫してサポートします~
お客様のお悩みやご要望に合わせて最適なサービスをご提案します。
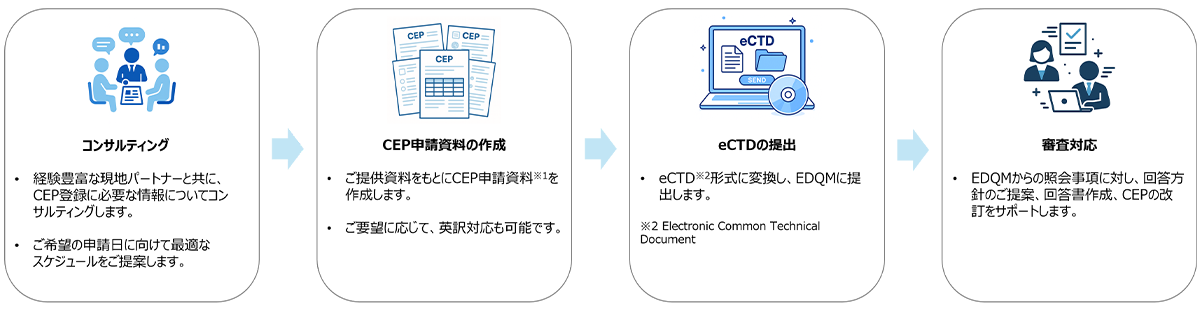
- ※1 CEPでは開示/非開示パートを分けて登録します。
2.その他サービス ~CEP登録後の維持・管理や、関連サポートも承ります~
変更手続き(Annual Notification、Immediate Notification、Minor change、Major change)
更新手続き(初回登録から5年目)
登録情報に変更が生じた場合に必要となる変更手続きも対応します。変更カテゴリー分けもお任せください。

データ取得のサポート
EP準拠試験など、CEP登録に必要なデータ取得をサポートします。

問い合わせ対応
ご不明な点がございましたら、何でもご相談ください。EDQMへの問い合わせも代行します。

当社の強み

現地パートナーとの強力な連携
欧州現地の信頼できる複数のパートナーと協力し、迅速かつ的確に対応します。

専門家によるコンサルティング
医薬品の製造・品質管理・薬事など多様なバックグラウンドを持つ専門家が、最適な解決策をご提案します。

豊富な実績
欧州に新規参入されるお客様を含め、様々な業種のお客様からCEP登録のご依頼をいただいています。

厳格な品質管理
徹底したQCチェックにより信頼性の高いサービスをご提供します。
よくあるご質問
Q.CEP登録は初めてですが、大丈夫でしょうか?
A. はい、欧州薬事規制の基礎から必要な記載情報まで、分かりやすくご説明しながらサポートします。
Q.CEP登録に必要な準備期間はどれくらいですか?
A. 正式にご依頼いただいてから概ね1年ぐらいで登録可能ですが、データの充足度によって異なるため、ヒアリングを元に最短、最適なプランをご提示します。米国にDMFを登録済の場合は半年程度で登録可能です。
Q.CEP登録に必要な資料は何でしょうか?
A.CEP登録には、まずCTDモジュール3に該当する資料が必要となりますが、すべての資料がご依頼時に揃っている必要はございません。ご提供いただいた資料をもとに、必要に応じてコンサルティングを行いながら、登録に向けてサポートします。
Q.申請後、当局からどんな照会を受けるかわからないので不安です。
A.現地パートナーと協議しながら照会回答の作成もサポートします。審査対応も実績がありますので、安心してお任せください。
Q.具体的な相談の前に料金を知りたいです。
A.CEP登録される製品の種類や資料のボリューム、ご希望されるサービス内容によるため、ヒアリングをさせていただいた上でお見積りをご提示しています。まずはお問い合わせフォームよりご連絡ください。ご予算に応じたサービスをご提案します。
関連サービス
新有効成分のDMF(ASMF)登録については以下を参照ください。
米国向けDMF登録については以下を参照ください。
中国向けDMF登録については以下を参照ください。
技術事例
お問い合わせ・ご相談
