化学的キャラクタリゼーション、溶出物の評価

医療機器の生体適合性評価では、主に医療機器や原材料から溶出する化学物質の生体への有害性が評価されます。溶出物の定性的、定量的な評価は、生物学的安全性試験の実施の必要性の判断等における有用な材料となります。また、医療機器は水や消毒剤などの様々な溶液と接触します。その溶出特性は、製品の品質の観点でも重要です。
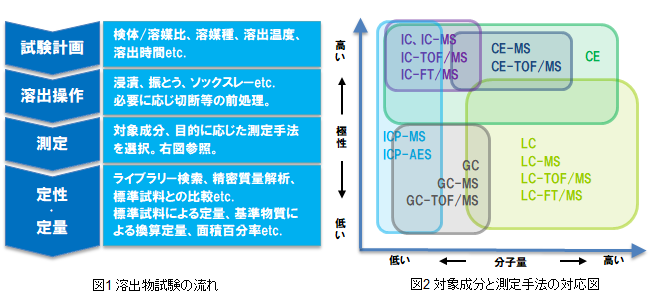
実際の溶出物試験では、試験計画から始まり、溶出操作、測定、定性・定量と進めますが(図1)、溶出操作によって得られる溶出物は多種多様な化学物質であることから、各物質の性質に合った測定手法を駆使して定性・定量を行います(図2)。
ISO 10993-18 に基づく ケミカルキャラクタリゼーション
医療機器の生物学的安全性評価は、国際標準規格であるISO 10993-1:2025に基づき実施されます。2025年11月に改訂された最新のISO 10993-1:2025では、申請対象となる医療機器に対して、生物学的安全性リスクアセスメントを行い、評価対象ごとに要求されるエンドポイントや試験の要否を確認し、必要に応じて試験を実施することが求められています。
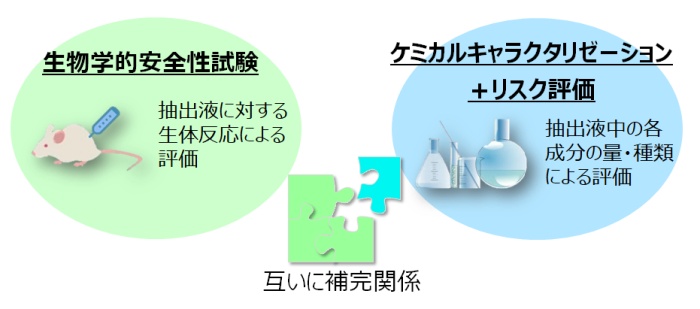
医療機器を構成する各部材の物理学的・化学的情報の収集は生物学的安全性評価の1st stepであり、生体に影響を及ぼすリスク因子を明らかにする目的でISO 10993-18:2020に規定された医療機器に由来する溶出物(Extractables/Leachables:抽出物/浸出物)の評価(Chemical Characterization:化学的キャラクタリゼーション)を用いて各部材から溶出する成分の情報を取得することは、生物学的安全性評価において不可欠であると位置付けられています。
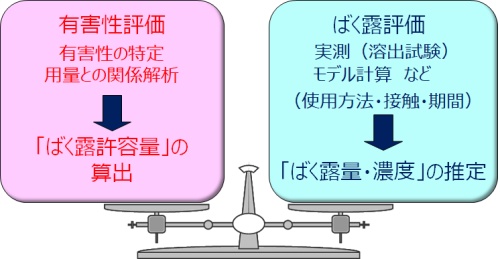
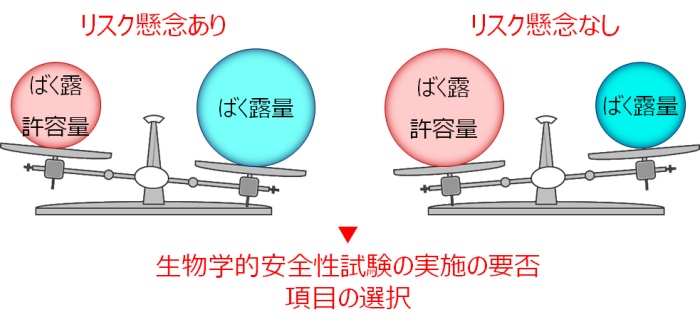
また、医療機器に対する定性的・定量的な溶出物分析は、溶出した化学物質の有害性評価と組み合わせることによって、機器から浸出する恐れのある物質のリスクアセスメント(毒性学的閾値ならびに摂取許容値に基づく安全性評価)を可能にし、新たな生物学的安全性試験の実施の要否を決定するための判断材料とすることができます。
当社は、医療機器および原材料(高分子化合物、金属、セラミックス等)の化学分析と化学物質の毒性調査・評価をはじめとした、国際標準であるISO 10993-1:2025の枠組みに沿ったケミカルキャラクタリゼーションとリスクアセスメントを提供します。
化学物質の定量的リスク評価の概念
ケミカルキャラクタリゼーションをはじめとした溶出試験やリスクアセスメントに関する技術資料をご用意しております。
ご希望の方は以下の"資料請求"ボタンをクリックし、お客様情報入力フォームよりお申し込みください。
技術事例
お問い合わせ・ご相談
