医療機器の毒性学的リスクアセスメント

当社では、最新のガイドラインと日米欧の3極申請に対応した医療機器の毒性学的リスクアセスメントサービスを提供いたします。
医療機器最終製品は、リスクマネジメントプロセスの一環としてISO10993-1に従い生物学的安全性評価が必要とされています。
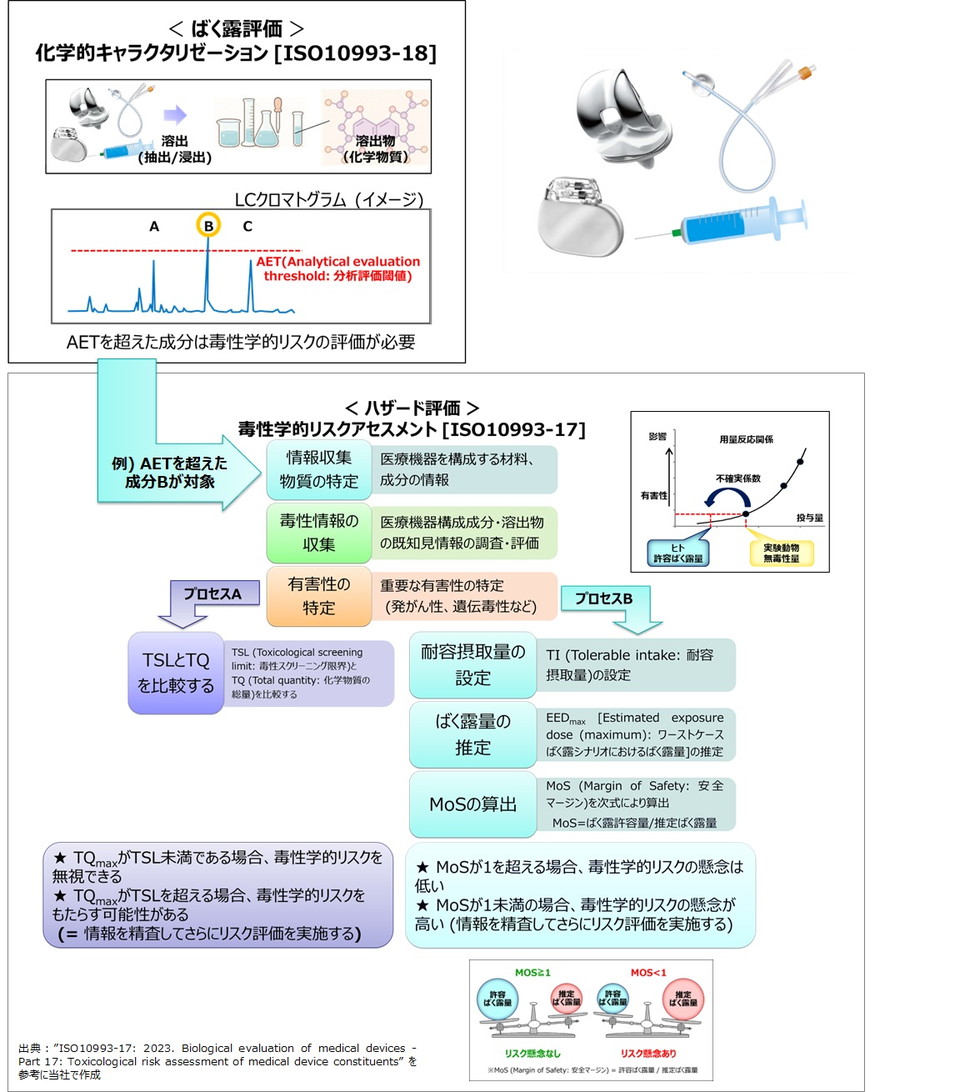
評価ではISO10993-18に基づいて成分情報(構成材料、添加物、溶出される成分など)を取得し、必要に応じてISO10993-17に従った毒性学的リスクアセスメントを実施します。
当社には、医療機器分野で豊富な経験を有するリスク評価の専門家がおり、毒性学的リスクアセスメントについても多数の受託実績がございます。
医療機器の特性や用途に応じて、専門家が最適な毒性学的リスクアセスメントの進め方をご提案し、最新の科学的知見と規制動向を踏まえた「毒性学的リスクアセスメント報告書」を作成します。
適用ガイドライン
- ISO10993-1: 2025. "Requirements and general principles for the evaluation of biological safety within a risk management process."
- ISO10993-17: 2023. "Biological evaluation of medical devices - Part 17: Toxicological risk assessment of medical device constituents"
- ISO/TS21726: 2019. "Biological evaluation of medical devices - Application of the threshold of toxicological concern (TTC) for assessing biocompatibility of medical device constituents."
- PMDA (Pharmaceuticals and Medical Devices Agency: 独立行政法人 医薬品医療機器総合機構). 生物学的安全性評価の審査ポイント, 2025年6月4日
- 厚生労働省. 「医療機器の製造販売承認申請等に必要な生物学的安全性評価の基本的考え方についての改正について」の全部改正について (令和7年3月11日付け、医薬機審発0311第1号厚生労働省医薬局医療機器審査管理課長通知)
ご相談やご依頼につきましては、用途やご要望に合わせて丁寧に対応いたします。
リスク評価に関するご質問やご相談がございましたら、お気軽にお問い合わせください。
技術事例
お問い合わせ・ご相談
