医薬品・医療機器申請支援

国内向けの医薬品・医療機器の申請支援、コンサルティングから、海外向けのマスターファイル(MF)登録まで、品質や申請に関わるあらゆるお悩みをご相談ください。
国内向け医薬品・医療機器の申請支援
医薬品や医療機器等の開発に関わる「分析試験の実施」から「製造販売の承認取得」まで一貫したサービスを提供します。
海外向けマスターファイル(MF)登録支援
現地パートナーと連携し、お客様のご要望に沿って、米国、欧州(EU)、中国向けマスターファイル(MF)登録をフルサポートします。
台湾などその他の国・地域も対応可能ですので、まずはご相談ください。
米国
欧州(EU)
中国
このようなお悩みはございませんか?
- エンドユーザーから詳細情報の開示を求められたが、製造ノウハウは開示したくない。
- MF登録をしたいが、どんな情報を記載したらよいのかよくわからない。
- 審査当局とのコミュニケーション(照会事項対応等)が不安。
- MF登録のため、各国で求められる試験(USP、中国薬局方、包装材料の中国YBB規定準拠試験など)を実施したい。
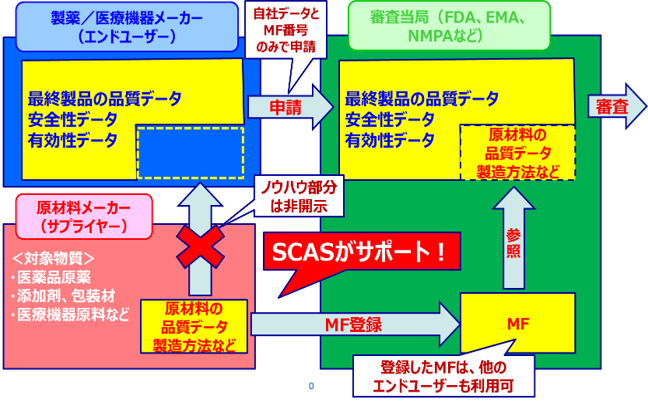
MF制度の概念図
お問い合わせ・ご相談








